En İyi Tedarikçiler, Çok Satan Na2SO4 %99 Susuz Sodyum Sülfat
Ayrıca, son derece rekabetçi bir ortamda en çok satan %99 saflıkta susuz sodyum sülfat (Na2SO4) ürünleri tedarikçisi olarak büyük kazanç sağlayabilmek için yönetim ve kalite kontrol programımızı iyileştirmeye odaklanıyoruz. Gelecekteki iş ilişkileri ve karşılıklı başarılar için her kesimden yeni ve eski müşterilerimizi bizimle iletişime geçmeye davet ediyoruz!
Rekabetin son derece yoğun olduğu bu sektörde büyük kazançlar elde edebilmek için, yönetim ve kalite kontrol programımızı iyileştirmeye de odaklanıyoruz. Şirketimiz "Önce Kalite, Sürdürülebilir Kalkınma" ilkesine bağlı kalmakta ve "Dürüst Ticaret, Karşılıklı Fayda"yı geliştirme hedefimiz olarak benimsemektedir. Tüm üyelerimiz, eski ve yeni tüm müşterilerimizin desteği için içtenlikle teşekkür eder. Çok çalışmaya ve size en yüksek kalitede ürün ve hizmet sunmaya devam edeceğiz.










 Sodyum Sülfür (Na₂S) Üretim Süreci
Sodyum Sülfür (Na₂S) Üretim Süreci
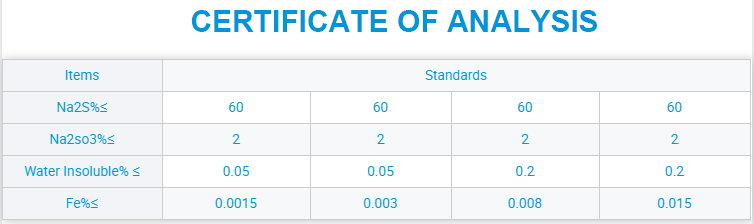
Na₂SO₄ otomatik bir besleyici vasıtasıyla bir hazneye beslenir ve daha sonra bir yanma odasına taşınır; burada sodyum sülfat üflenir ve kömür gazı kullanılarak yakılır. Sıcaklık 884°C'ye ulaştığında, sodyum sülfat sıvı hale gelir. Çözünmüş Na₂SO₄ kimyasal olarak kararsız hale gelir ve SO₄²⁻ iyonları kolayca ayrışır. Fosfor içeren kömür gazından elde edilen karbonmonoksit kullanılarak aşağıdaki gibi kimyasal bir yer değiştirme reaksiyonu gerçekleşir:
Na₂SO₄ + 4CO → Na₂S + 4CO₂
Fırındaki alev maviden kırmızıya döndüğünde, CO ile yer değiştirme reaksiyonu tamamlanmıştır. Bu noktadan sonra, CO yalnızca sıcaklığı daha da artırmak için yakıt görevi görür. Sıcaklık 1100°C'ye ulaştığında, az miktarda antrasit eklenir. Reaksiyonun son noktası, fırın içinde sarı, parıldayan bir alevin görünmesiyle belirtilir. Kimyasal reaksiyon şu şekildedir:
Na₂SO₄ + 2C → Na₂S + 2CO₂
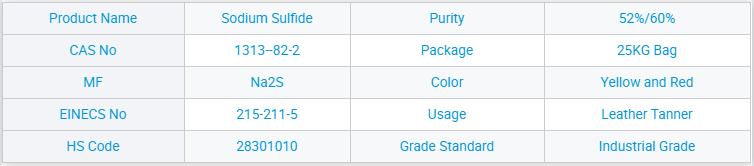
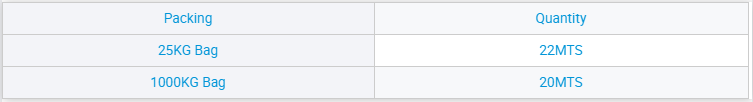
Sodyum Sülfat.




















